Эндокринная офтальмопатия (ЭОП) представляет собой аутоиммунное заболевание с широким спектром клинических проявлений, как правило, ассоциированное с гипертиреозом Грейвса. Диагностика основывается на сборе анамнеза и физикальном осмотре, однако при неясных случаях могут применяться дополнительные методы исследования.
ЭОП является наиболее частой причиной одностороннего и двустороннего экзофтальма у взрослых и чаще всего диагностируется у женщин в возрасте от 30 до 50 лет. Несмотря на это, тяжесть течения заболевания более выражена у мужчин, а также у пациентов, впервые выявленных в возрасте старше 50 лет. По оценкам, заболеваемость ЭОП составляет 16 женщин и трое мужчин на 100 000 населения в год.
К факторам риска относят курение, пожилой возраст на момент диагностики гипертиреоза Грейвса, длительное течение гипертиреоза, неконтролируемую дисфункцию щитовидной железы и предшествующее лечение радиоактивным йодом.
Течение ЭОП является двухфазным: прогрессивная (активная) фаза, которая может длиться до трех лет, сменяется стабильной (неактивной) фазой. Офтальмологические проявления варьируют от легких до угрожающих зрению, а тактика лечения — от поддерживающей терапии до хирургического вмешательства — зависит от степени тяжести.
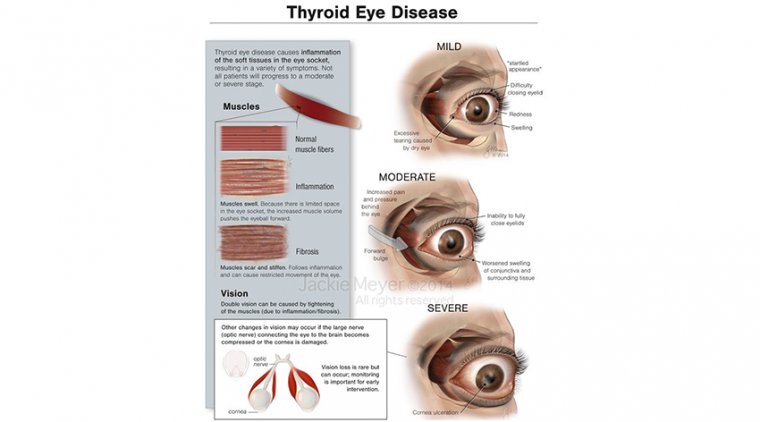
Клинические признаки включают ретракцию века, периорбитальный отек, инъекцию конъюнктивы и хемоз, экзофтальм, ограничение подвижности глазодвигательных мышц, кератопатию, обусловленную экспозицией роговицы, и компрессионную оптическую нейропатию. Разнообразие клинических проявлений обусловливает широкий круг дифференциального диагноза (аллергический конъюнктивит, орбитальные опухоли), что требует междисциплинарного подхода к ведению пациентов с ЭОП.
Молекулярный механизм аутоиммунного процесса при ЭОП является многофакторным. При болезни Грейвса наблюдается гиперэкспрессия рецептора тиреотропного гормона (РТТГ) в ретробульбарных тканях. При активации РТТГ орбитальные фибробласты пролиферируют и секретируют провоспалительные цитокины и гидрофильный гиалуронан в интерстициальное пространство. Это создает значительные осмотические градиенты на орбите, приводя к накоплению жидкости. Кроме того, часть орбитальных фибробластов дифференцируется в зрелые адипоциты, вызывая расширение орбитальной жировой ткани. Данные изменения приводят к атрофии, фиброзу и склерозу глазодвигательных мышц и могут вызывать ограничительное косоглазие.
Для классификации ЭОП используется несколько инструментов. Первый — мнемоническое правило NO SPECS, созданное в 1969 году, которое перечисляет клинические признаки ЭОП, однако оно не является хорошим индикатором тяжести и прогрессирования заболевания. В 1989 году Моуритис с соавторами предложили шкалу клинической активности (CAS), которая характеризует активную и неактивную стадии. В 2008 году Европейская группа по изучению орбитопатии Грейвса (EUGOGO) обновила рекомендации по ведению пациентов с учетом результатов клинических исследований.
Клиническая оценка при ЭОП включает сбор анамнеза, физикальное обследование, биохимический анализ крови и инструментальную визуализацию (по показаниям). Общие клинические признаки — ретракция верхнего века, инъекция и/или отек конъюнктивы и слезного мясца, отек и/или эритема век с суточными колебаниями, нарушение подвижности глаз и косоглазие, экзофтальм. Оценка фокусируется на определении активности и тяжести процесса путем исследования остроты зрения, реакции зрачков, цветоощущения, движений глазных яблок, полей зрения, экзофтальмометрии, осмотра век, биомикроскопии и офтальмоскопии с осмотром глазного дна.
Дополнительная диагностика включает биохимический скрининг дисфункции щитовидной железы (важно отметить, что некоторые пациенты с ЭОП могут быть эутиреоидны). В таких случаях проводятся лабораторные тесты на антитела к рецептору ТТГ (TRAb), тиреоидстимулирующие иммуноглобулины (TSI) и антитела к тиреоидной пероксидазе (TPO).
Методы визуализации орбиты, такие как ультразвуковое исследование, компьютерная томография (КТ) и магнитно-резонансная томография (МРТ), помогают подтвердить ЭОП и исключить другие дифференциальные диагнозы. Наиболее популярна КТ без контрастирования, так как она позволяет визуализировать костные структуры орбиты и является более экономически эффективной по сравнению с МРТ. На КТ-сканах орбиты можно выявить характерные для ЭОП изменения, такие как увеличение мышечных брюшок глазодвигательных мышц с сохранением сухожилий. Типично асимметричное двустороннее вовлечение глазодвигательных мышц в следующем порядке: нижняя прямая, медиальная прямая, верхняя прямая, латеральная прямая и косые мышцы. При подозрении на компрессионную оптическую нейропатию вследствие апикального сдавления МРТ является золотым стандартом визуализации.
Оптимальное ведение дисфункции щитовидной железы требует междисциплинарного подхода. Первоочередная цель лечения — восстановление и поддержание эутиреоидного состояния. Основные методы лечения: антитиреоидные препараты, тиреоидэктомия и радиоактивный йод. Ведутся споры о применении радиоактивного йода, поскольку он может усугубить ЭОП; некоторые источники рекомендуют применение кортикостероидов после радиотерапии для снижения риска развития или прогрессирования ЭОП.
Отказ от курения является наиболее важным модифицируемым фактором риска в профилактике и прогрессировании ЭОП. EUGOGO рекомендует отказ от курения всем пациентам с ЭОП независимо от тяжести заболевания. Консервативное лечение включает увлажняющие препараты без консервантов, увлажняющие камеры и заклеивание век при синдроме сухого глаза. Солнцезащитные очки помогают при светобоязни и бликах. При диплопии в активной фазе помогают призмы или монокулярная окклюзия. При диплопии в неактивной фазе может использоваться призматическая коррекция в очках. Инъекции ботулотоксина в комплекс мышцы, поднимающей верхнее веко, и мышцы Мюллера могут быть использованы для уменьшения ретракции верхнего века.
Орбитальное облучение применяется при ЭОП, однако его роль остается спорной. Обычно оно хорошо переносится и безопасно, но относительно противопоказано пациентам моложе 35 лет или с сосудистыми заболеваниями. Орбитальное облучение снижает скорость пролиферации орбитальных фибробластов, уменьшая отек. Пациенты с компрессионной оптической нейропатией и/или тяжелой экспозицией роговицы имеют угрожающую зрению форму ЭОП. Раннее распознавание таких пациентов критически важно для своевременного лечения. Необъяснимое ухудшение зрения, изменение цветоощущения на один или оба глаза, сублюксация глазного яблока, помутнение роговицы, недавнее появление хориоидальных складок и отек диска зрительного нерва указывают на угрожающую зрению эндокринную офтальмопатию.
Рекомендация EUGOGO для пациентов с компрессионной оптической нейропатией включает высокие дозы внутривенных кортикостероидов с последующей срочной орбитальной декомпрессией при слабом ответе или его отсутствии на кортикостероиды. В тяжелых случаях экспозиции роговицы частые увлажняющие препараты могут быть недостаточны для предотвращения изъязвления, истончения и перфорации. В таких случаях могут использоваться увлажняющие камеры, местный циклоспорин, местные или субконъюнктивальные кортикостероиды, мягкие бандажные контактные линзы, лечебные склеральные контактные линзы, амниотические мембраны или тарзорафия для стимуляции заживления роговицы.
Хирургическая реабилитация показана пациентам с умеренно-тяжелой неактивной эндокринной офтальмопатией при значительном влиянии на зрительные функции или качество жизни. Общая хирургическая последовательность при неактивной ЭОП: сначала орбитальная декомпрессия, затем хирургия глазодвигательных мышц, и в последнюю очередь — операции на веках. Экспозиционная кератопатия может лечиться временной тарзорафией в ожидании орбитальной декомпрессии. Хирургия глазодвигательных мышц (косоглазия) рассматривается в случаях, когда диплопия сохраняется или ухудшается после орбитальной декомпрессии. Хирургия век выполняется последней при симптоматической ретракции века или асимметричном положении век с целью поддержания адекватного покрытия роговицы.