Географическая атрофия (ГА) представляет собой позднюю форму возрастной макулярной дегенерации (ВМД), при которой поражается сетчатка — структура глаза, передающая зрительную информацию в головной мозг. Многие пациенты с ВМД не сразу распознают симптомы, ошибочно принимая их за обычные возрастные изменения, что приводит к более выраженной потере зрения. При ГА острота зрения может оставаться высокой, если макула (центральная область сетчатки, отвечающая за резкое центральное зрение) не затронута. По состоянию на апрель 2021 года не существовало методов лечения, замедляющих прогрессирование ГА, однако проводились клинические исследования потенциальных терапевтических средств. В качестве вспомогательных средств могли назначаться устройства для слабовидящих, такие как лупы или специальные очки.
ГА влияет на способность выполнять социальные и бытовые действия: распознавать лица, водить автомобиль, читать, находить уличные указатели. В литературе влажная и сухая формы ВМД ассоциировались со снижением мобильности и способности к вождению. Пациенты с распространённой сухой формой ВМД (ГА) также сообщали о снижении способности к чтению, социальной изоляции и невозможности поддерживать личную гигиену. Отмечалось снижение уверенности при выполнении повседневных задач, которые ранее не вызывали затруднений. Например, среди пациентов с ГА, имеющих водительские права, 50% сообщали о неуверенности при дневном вождении и 88% — при ночном.
Учитывая влияние на качество жизни, пациенты ставили тяжёлую (острота зрения 20/200) и очень тяжёлую (острота зрения 20/800) потерю зрения вследствие ВМД в один ряд с такими тяжёлыми состояниями, как домашний диализ, некупируемая боль при раке или инсульт, приводящий к постоянному постельному режиму. По оценкам, к 2030 году в США насчитывалось более 3,5 млн пациентов с ВМД, а к 2050 году это число должно было достигнуть 5 млн. С увеличением числа пациентов в клиниках и при появлении методов лечения ГА важным становилось понимание классификации заболевания, методов количественной оценки его прогрессирования и оптимальных способов оценки зрительных нарушений, вызванных ГА. Это позволяло изучать эффекты и исходы потенциальных терапевтических средств, а также выявлять пациентов с высоким риском прогрессирования, которые могли бы получить максимальную пользу от раннего вмешательства.
Классификация и факторы риска ГА
Комитет по классификации Инициативы Beckman по исследованию макулы разделил ВМД на четыре стадии: (1) отсутствие ВМД; (2) ранняя ВМД; (3) промежуточная ВМД; (4) поздняя ВМД. Двумя формами поздней ВМД являются неоваскулярная (влажная) ВМД и ГА. Отсутствие ВМД диагностировалось при отсутствии пигментных аномалий и наличии единичных мелких друз (менее 63 мкм). При ранней ВМД пигментные изменения отсутствовали, размер друз составлял от 63 до 125 мкм. Наличие хотя бы одной друзы более 125 мкм или пигментные изменения соответствовали промежуточной ВМД (в клинике полезно использовать центральную вену сетчатки диаметром около 125 мкм для измерения друз). Центральная потеря зрения, связанная с повреждением макулы, являлась признаком поздней ВМД. При наличии неоваскуляризации диагностировалась влажная ВМД. У пациентов с ГА наблюдалась потеря фоторецепторов, истончение слоёв пигментного эпителия сетчатки (ПЭС) и хориокапилляров, а также формирование плотных скотом.
Курение и возраст были связаны с развитием ГА. Анамнез курения 40 пачек-лет ассоциировался с 3,4-кратным повышением риска развития ГА. У пациентов старше 90 лет распространённость ГА была значительно выше, чем у пациентов 84 лет и моложе. Факторами риска развития ВМД в целом являлись семейный анамнез ВМД, курение, ожирение и артериальная гипертензия.
Клиническая картина
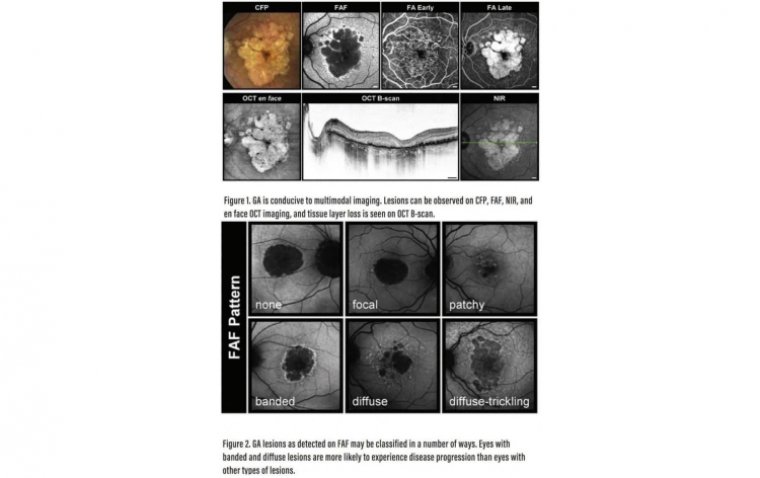
ГА можно было визуализировать с помощью ряда методов (Рисунок 1). Отчёты по визуализации могли служить удобным инструментом для информирования пациентов и их семей о прогрессировании заболевания, выявления пациентов с наибольшим риском прогрессирования, а также для оценки эффектов потенциальных терапевтических средств. Наиболее часто используемыми методами визуализации в клинической практике и исследованиях были оптическая когерентная томография (ОКТ), цветная фотосъёмка глазного дна (ЦФГ) и аутофлуоресценция глазного дна (АФ). Изучалась роль таких методов, как ОКТ-ангиография и конфокальная ближняя инфракрасная рефлектометрия. В-сканирование ОКТ чаще всего использовалось врачами в клинике; оно демонстрировало потерю наружных слоёв сетчатки, соответствующих ПЭС и фоторецепторам. En face ОКТ могла использоваться для обучения пациентов. ЦФГ применялась в более ранних клинических исследованиях, в то время как АФ стала современным основным методом оценки ГА. ЦФГ показывала чётко очерченные гипопигментированные унифокальные или мультифокальные зоны, иногда с видимыми более крупными хориоидальными сосудами из-за отсутствия ПЭС и хориокапилляров. Прогрессирование обычно начиналось в экстрафовеолярной области и распространялось по подковообразному типу, пока поражение не приобретало форму пончика. Фовеолярное вовлечение обычно происходило на конечной стадии прогрессирования. Визуализация очагов ГА была важна для выявления пациентов с высоким риском прогрессирования и отслеживания анатомических исходов будущего лечения.
Исследования естественного течения заболевания определили, что скорость прогрессирования очагов у пациентов с ГА составляла от 0,53 мм² до 2,6 мм² в год (медиана 1,78 мм²). Факторами более быстрого прогрессирования являлись больший исходный размер очага, экстрафовеолярные очаги, мультифокальные очаги, ГА на парном глазу, а также некоторые паттерны АФ. На АФ гипоаутофлуоресцентные зоны указывали на очаги ГА. Очаги могли иметь различную конфигурацию, а их границы или переходные зоны могли быть гипераутофлуоресцентными. Различные паттерны АФ рассматривались как фактор риска прогрессирования ГА. Holz с соавт. обнаружили, что у пациентов с ГА, чьи очаги классифицировались как полосчатые или диффузно-струящиеся, прогрессирование заболевания было более вероятным по сравнению с пациентами, чьи очаги соответствовали другим классификациям. Повышенная АФ в переходной зоне ГА могла классифицироваться как очаговая, пятнистая, полосчатая или диффузная, при этом диффузно-струящийся тип являлся одним из диффузных паттернов (Рисунок 2). При очаговых поражениях наблюдалось одно или несколько мелких пятен повышенной АФ на краю очага, тогда как очаги с некоторыми пятнами АФ за пределами зоны ГА классифицировались как пятнистые. Полосчатые паттерны определялись как центральная гипоаутофлуоресценция с гипераутофлуоресцентной границей, окружающей весь очаг. При диффузных очагах наблюдались пятна АФ за пределами зоны ГА с распространением к заднему полюсу. Очаги, демонстрирующие серую (а не чёрную) гипоаутофлуоресценцию и дольчатые атрофические участки с высокой интенсивностью по краям, классифицировались как диффузно-струящиеся.
Измерение зрительных потерь
Стандартная максимально корригированная острота зрения (МКОЗ) по таблицам Снеллена могла быть недостаточным измерением зрительной функции у пациентов с ГА из-за фовеалосохраняющего характера заболевания. Она не отражала реальный зрительный опыт пациента, и для оценки эффективности будущих методов лечения требовалось использование альтернативных методов, таких как микропериметрия, острота зрения при низкой освещённости (ОЗН), оценка скорости чтения и опросники с участием пациентов.
Микропериметрия
Микропериметрия измеряла пороговую светочувствительность во множестве точек над макулой. Во время теста пациент нажимал кнопку в ответ на восприятие стимула. Изменяя интенсивность стимула, можно было получить карту чувствительности. Данные о чувствительности поля зрения могли накладываться на ЦФГ и другие методы визуализации, что позволяло понять взаимосвязь между анатомией и функцией.
Острота зрения при низкой освещённости
Поскольку пациенты с ГА часто испытывали значительные нарушения зрения в условиях низкой освещённости, использование ОЗН могло быть надёжным показателем прогрессирования заболевания и его влияния на остроту зрения. При оценке ОЗН пациент читал нормально освещённую таблицу ETDRS через нейтральный светофильтр плотностью 2,0 log единицы, помещённый поверх максимальной коррекции для глаза. Sunness с соавт. обнаружили, что исходный дефицит при низкой освещённости был сильным предиктором последующей потери зрения для всех уровней исходной остроты зрения у пациентов с ГА. Они также выявили, что использование ОЗН могло идентифицировать пациентов с наибольшим риском потери остроты зрения вследствие ГА.
Оценка скорости чтения
Пациенты с экстрафовеолярными очагами ГА могли видеть отдельные буквы на традиционной таблице, поскольку одна буква могла попадать в фовеолярную область. Поэтому просьба к пациенту прочитать целое предложение могла быть более точным измерением зрительной функции. Такие оценки скорости чтения могли выявить снижение зрительной функции из-за парафовеолярных атрофических зон.
Опросники с участием пациентов
Опросник Национального института глаза по зрительной функции (NEI VFQ-25) являлся одним из примеров метода, с помощью которого пациенты могли сообщать о практической зрительной функции. Он включал вопросы, например, о способности выполнять повседневные задачи. Sivaprasad с соавт. обнаружили, что NEI VFQ-25 был надёжным и валидным одномоментным инструментом для оценки влияния ГА на зрительную функцию и связанное со зрением качество жизни пациентов.
Освоение оценки ГА
Если бы какая-либо из разрабатываемых терапий ГА получила одобрение регулирующих органов, это изменило бы парадигму ведения пациентов с ГА. Уже тогда понимание того, как нарушение зрения у пациента влияет на качество жизни, было важным. Учитывая, что потенциальные методы лечения могли предотвращать рост ГА, а не обращать вспять уже существующее повреждение, было особенно важно знать, как выявлять пациентов, которые получат наибольшую пользу от этих новых методов лечения, и как оценивать ответ на терапию.