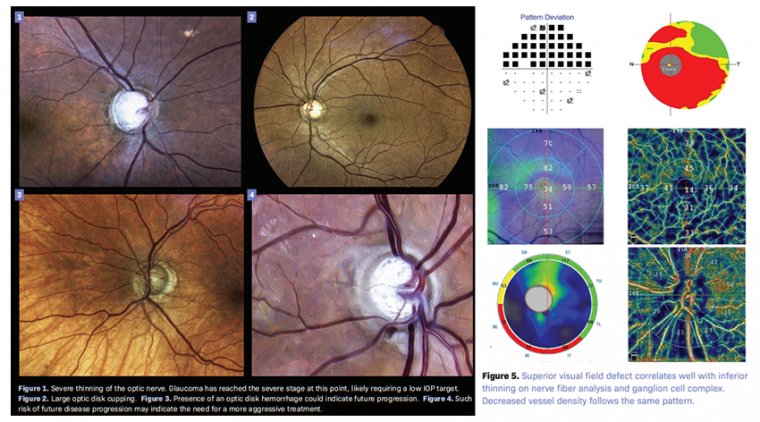
Глаукоматозная оптическая нейропатия, характеризующаяся прогрессирующей гибелью ганглиозных клеток сетчатки и их аксонов, приводит к структурно-функциональным повреждениям зрительного нерва, снижению зрения и слепоте. Первичная зона поражения, по-видимому, локализуется в решетчатой пластинке, где начальное повреждение проявляется в виде нарушения аксоплазматического тока, сопровождающегося прогрессирующей ламинопатией и транссинаптической дегенерацией.
Структурные изменения ганглиозных клеток сетчатки и их аксонов клинически визуализируются как альтерации слоя нервных волокон сетчатки и топографии диска зрительного нерва. Эти изменения могут быть зафиксированы с помощью компьютерных устройств, таких как спектральная оптическая когерентная томография макулы, слоя нервных волокон, диска зрительного нерва и решетчатой пластинки, что облегчает диагностику, мониторинг и лечение.
К факторам риска развития и прогрессирования открытоугольной глаукомы относятся системные и окулярные факторы: пожилой возраст, низкое перфузионное давление глаза, африканское или латиноамериканское происхождение, внутриглазное давление, оскольчатое кровоизлияние в головке зрительного нерва, тонкая центральная роговица, бета-зона парапапиллярной атрофии и эксфолиативный синдром.
Будучи самой частой причиной необратимой слепоты в мире, глаукоматозная оптическая нейропатия хорошо известна оптометристам, и клиницисты уверенно проводят ее диагностику и лечение. На протяжении многих лет стандартный алгоритм лечения оставался практически неизменным: местные лекарственные препараты до тех пор, пока заболевание не становилось достаточно тяжелым, чтобы рассматривать инцизионную хирургию. Однако в последнее десятилетие эта стратегия претерпела кардинальные изменения благодаря внедрению нескольких новых лекарственных средств, пересмотру роли лазеров и быстрому развитию малорисковых микрохирургических вмешательств. Диагностика глаукомы за последние годы прогрессировала лишь незначительно, в то время как ведение заболевания претерпело трансформацию: акцент сместился в сторону более раннего, более безопасного и зачастую более хирургического вмешательства.
В настоящей статье, являющейся первой частью двухчастного цикла, рассмотрены новые лекарственные препараты и применение лазеров. Вторая часть будет посвящена минимально инвазивной хирургии глаукомы.
Подходы к лечению
Глаукома — это хроническая прогрессирующая оптическая нейропатия, вызывающая необратимую потерю периферического и/или центрального зрения и в конечном итоге способная привести к слепоте. По оценкам, во всем мире глаукомой страдают около 76 миллионов человек, и в ближайшие два десятилетия это число будет расти. К факторам риска относятся пожилой возраст, семейный анамнез глаукомы, новая раса, тонкая роговица и повышенное внутриглазное давление.
Существует много подтипов глаукомы. Единственным модифицируемым фактором риска для большинства подтипов является повышенное внутриглазное давление, и практически все существующие методы лечения направлены на его снижение. Лечение глаукомы стандартизировать сложно, и решения подбираются индивидуально. Многие врачи устанавливают целевое внутриглазное давление для каждого глаза, которое затем служит ориентиром для терапии, поскольку считается максимально допустимым уровнем, вероятно предотвращающим или замедляющим дальнейшее ухудшение зрения.
Селективная лазерная трабекулопластика
Селективная лазерная трабекулопластика (СЛТ) — это лазер на неодимовом иттрий-алюминиевом гранате с модулированной добротностью и удвоением частоты (длина волны 532 нм), который доставляет очень короткие импульсы энергии к пигментированным клеткам трабекулярной сети. Структурных или коагуляционных повреждений трабекулярной сети после лечения не выявлено, процедура безболезненна и приводит в среднем к снижению внутриглазного давления на 17-30%. СЛТ показана при легких и средних формах открытоугольной глаукомы, пигментной дисперсии или псевдоэксфолиативной глаукомы.
После внедрения СЛТ в 2001 году врачи в США рассматривали ее как метод второй линии после неэффективности максимальной гипотензивной терапии, обычно непосредственно перед необходимостью инцизионной хирургии. Эта ситуация изменилась с публикацией в 2019 году исследования LiGHT, в котором исследователи убедительно доказали превосходство СЛТ над местными препаратами по эффективности, безопасности и стоимости, настоятельно рекомендовав рассматривать СЛТ перед началом инстилляций каких-либо капель. После обнародования выводов этого знакового исследования оптометристы и офтальмологи скорректировали свой лечебный алгоритм: теперь диагноз глаукомы часто влечет за собой первичное применение СЛТ вместо местных препаратов. Удовлетворенность пациентов СЛТ выше, чем каплями, а проблема приверженности лечению снимается. СЛТ можно повторять так часто, как необходимо, причем повторные процедуры часто демонстрируют большую эффективность.
Местные лекарственные препараты
Традиционно местные препараты считались терапией первой линии для пациентов с глаукомой. В настоящее время существует 5 основных категорий глазных капель, снижающих внутриглазное давление: аналоги простагландинов, ингибиторы -киназы, -блокаторы, -агонисты и ингибиторы карбоангидразы. Аналоги простагландинов (ПГА) снижают внутриглазное давление за счет уменьшения сопротивления оттоку в увеосклеральном пути. ПГА остаются препаратами первой линии благодаря своей эффективности, режиму дозирования один раз в день, доступности и низкому риску побочных эффектов. Применение ПГА коррелирует со снижением числа выполняемых трабекулэктомий.
Новые гипотензивные средства
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) недавно одобрило три новых местных препарата для лечения глаукомы, которые существенно повлияли на структуру назначений. Первым из них был латанопростен буноид (Vyzulta, Bausch + Lomb), выпущенный в 2017 году. Он сочетает известный агент латанопрост с оксидом азота, который увеличивает отток водянистой влаги за счет расслабления хронического сокращения трабекулярной сети. Это обеспечивает снижение внутриглазного давления на 1-2 мм рт.ст. больше, чем при использовании одного ПГА, сохраняя тот же режим дозирования.
Нетарсудил 0,2% (Rhopressa, Aerie Pharmaceuticals), ингибитор -киназы, также был представлен в 2017 году. Фермент -киназа способствует сокращению клеток трабекулярной сети и матрикса, поэтому ингибирование этого фермента препаратом увеличивает отток водянистой влаги через трабекулярную сеть. Применение нетарсудила вызывает конъюнктивальную гиперемию у 50% пациентов. Нетарсудил комбинируется с латанопростом в препарате Rocklatan (Aerie), который обеспечивает самое высокое среднее снижение внутриглазного давления среди всех монопрепаратов для лечения глаукомы: на 30-36% от исходного уровня. Режим инстилляций идентичен ПГА, латанопростену буноиду и нетарсудилу: один раз в день на ночь.
Внедрение нетарсудила и оксида азота существенно изменило лечебный алгоритм. Многие врачи по-прежнему начинают местную терапию с ПГА, но если этот препарат оказывается недостаточно эффективным, они могут рассмотреть переход на Vyzulta или Rocklatan.
Традиционные гипотензивные средства
Более старые местные препараты все еще могут играть полезную роль в снижении внутриглазного давления. К ним относятся -блокаторы, -агонисты и ингибиторы карбоангидразы. -Блокаторы снижают внутриглазное давление за счет уменьшения продукции водянистой влаги, их следует избегать у пациентов с брадикардией, гипотензией, астмой и обструктивными заболеваниями легких.
Ингибиторы карбоангидразы и -агонисты обычно используются в качестве средств второй линии. К сожалению, увеличение количества ежедневно применяемых капель негативно влияет на приверженность пациентов лечению. По данным некоторых исследований, менее 50% пациентов продолжают соблюдать терапию после первого года. Комбинированная терапия может помочь приверженности и уменьшить воздействие консервантов. Список комбинированных капель, доступных в США, включает тимолол плюс бримонидин (Combigan, Allergan), тимолол плюс дорзоламид (Cosopt/Cosopt PF, Akorn), бримонидин плюс бринзоламид (Simbrinza, Alcon) и Rocklatan.
Преодоление неприверженности терапии
Крупнейшим фактором, препятствующим успеху медикаментозного лечения глаукомы, является неспособность пациента соблюдать режим местной терапии. Проблемы включают трудности с закапыванием, побочные эффекты и стоимость лекарств. Всестороннее просвещение пациентов относительно серьезности и необратимости потенциальной потери зрения на удивление неэффективно. У молодых пациентов уровень неприверженности выше, несмотря на лучший доступ к информации о глаукоме. Лекарства с наиболее простым режимом введения (один раз в день) должны рассматриваться в качестве терапии первой линии.
Методы лечения, не зависящие от постоянного сотрудничества пациента, включают СЛТ, хирургические вмешательства и имплантаты с пролонгированным высвобождением. Единственным одобренным на данный момент устройством является интракамеральный имплантат с биматопростом Durysta (Allergan). Твердый биодеградируемый имплантат в форме стержня помещается в угол передней камеры и медленно высвобождает аналог простагландина по мере деградации его сополимерной матрицы. Имплантат способен доставлять лекарство до 6 месяцев, но пока не одобрен для повторного применения.
Новая парадигма
В лечении глаукомы происходит смена парадигмы: управление этим заболеванием сместилось в сторону более раннего, более безопасного и зачастую более хирургического вмешательства. Стало известно, что большая часть пациентов не использует глазные капли по назначению, а новая волна препаратов с однократным суточным дозированием и повышенное использование СЛТ-лазера в качестве терапии первой линии стали мощными стратегиями для достижения более стабильных результатов. По мере того как оптометристы осваивают новые возможности, удается предложить пациентам более высокий стандарт помощи, что может значительно уменьшить потерю зрения из-за этого заболевания.