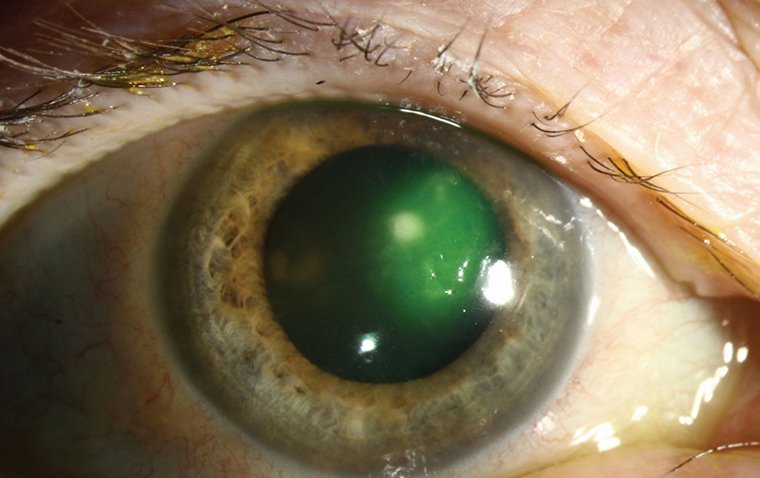
Ношение контактных линз в глобальных масштабах возросло за последние десятилетия, что является одним из основных факторов риска развития микробного кератита. Микробный кератит представляет собой тяжёлое и опасное состояние, вызывающее воспаление роговицы.
Потенциальные осложнения микробного кератита
При отсутствии лечения заболевание может привести к рубцеванию и перфорации роговицы, а также к эндофтальмиту и потере зрения. Среди бактериальных, грибковых, протозойных и вирусных агентов, способных вызывать микробный кератит, бактерии являются наиболее частой причиной.
Что такое эндофтальмит?
Эндофтальмит — это глазное заболевание, характеризующееся воспалением и болью внутри глаза. Оно вызывается инфекцией и может привести к тяжёлой потере зрения при отсутствии своевременного лечения.
Возбудители и этиология микробного кератита
Микробный кератит — это заболевание роговицы, которое включает различные патогены и этиологические факторы. Хотя микробный кератит, связанный с ношением контактных линз, чаще всего ассоциирован с бактериальными инфекциями, ответственными могут быть и другие патогены (грибы, виды Acanthamoeba и др.).
Ношение контактных линз и повышенный риск осложнений
Ношение контактных линз значительно повышает риск глазных осложнений, в частности микробного кератита, который является наиболее тяжёлым и угрожающим зрению осложнением. Термин «микробный кератит» включает бактериальный кератит, грибковый кератит и акантамёбный кератит. Бактериальный кератит — это инфекция роговицы, вызванная бактериями. Данное состояние может вызывать сильную боль, покраснение и воспаление, а при отсутствии лечения приводить к потере зрения или слепоте.
Географические различия в причинах микробного кератита
Географически причины микробного кератита различаются. В невестернизированных странах травма является ведущей причиной микробного кератита, тогда как в вестернизированных странах ношение контактных линз сопоставимо с травмой или даже превосходит её как наиболее значимый фактор. Микробный кератит служит основной причиной рубцевания роговицы и создаёт значительное экономическое бремя для системы здравоохранения, особенно на фоне роста использования контактных линз. Кроме того, задержка вмешательства связана с повышенным риском необходимости трансплантации роговицы.
Важность незамедлительного вмешательства и лечения
В связи с этим немедленная идентификация, соответствующее лечение и последующее наблюдение имеют решающее значение для успешных долгосрочных исходов. В статье представлен основанный на доказательствах алгоритм ведения типичных язв роговицы, чаще всего вызываемых видами Staphylococcus и Pseudomonas.
Сбор подробного анамнеза пациента
Рассказ пациента о временной динамике заболевания может дать ключ к определению возбудителя и его вирулентности. Передозировка контактных линз и плохая гигиена являются наиболее распространёнными факторами риска любого инфекционного кератита. Также выясняются сведения о предыдущих травмах или операциях, наличии заболеваний глазной поверхности, контакте с растительностью (работает ли пациент в сельском хозяйстве, садоводством и т.п.), поскольку это может повышать риск атипичных инфекций. Дополнительно определяется, не является ли пациент иммунокомпрометированным или не имеет ли риска нейротрофического кератита. Нейротрофический кератит может приводить к замедленному заживлению, даже если инфекция лечится правильно. Также собирается точная информация о предшествующем лечении пациента, особенно о применении местных кортикостероидов, которые могут существенно изменить внешний вид язвы и усилить патогенность атипичных инфекций.
Идентификация язвы роговицы
Процесс начинается с систематической оценки всего глаза и требует частых повторных осмотров для оценки вирулентности возбудителя. Центральные поражения вызывают больше беспокойства из-за их влияния на зрение. Быстро прогрессирующая некротизирующая суппурация стромы в большей степени указывает на бактериальную этиологию, тогда как более медленное прогрессирование может указывать на атипичные причины (вирусные, грибковые или протозойные). Тщательное измерение сопутствующего эпителиального дефекта, суппурации стромы, отёка и воспаления даёт полезную информацию о тяжести и прогрессировании язвы. Классические качественные ассоциации, такие как «пушистые» края и сателлитные очаги при грибковых инфекциях или кольцевидные инфильтраты при акантамёбном кератите, требуют дальнейшего обследования (дополнительные посевы, окрашивания или визуализация). Степень экстракорнеального воспаления, например вовлечение склеры и передней камеры, также должна быть отмечена как маркер тяжести и характеристика инфекции. Всегда следует учитывать воспалительное заболевание век и тщательно их осматривать. Если у пациента имеются двусторонние язвы, а прямая причина (например, ношение контактных линз) не очевидна, следует рассмотреть системное обследование на дефицит витамина A, ВИЧ или другие иммунодефицитные состояния. Данные обследования могут быть сложными, поэтому врач первичного звена обычно может помочь с назначением соответствующих анализов крови.
Определение соответствующего лечения
Для определения тактики лечения микробного кератита используется двухуровневая система классификации риска (низкий или высокий риск) согласно клиническим рекомендациям Американской академии офтальмологии (AAO) по бактериальному кератиту. Микробный кератит низкого риска: это небольшие, периферические или парацентральные, не угрожающие зрению язвы. Рекомендации AAO определяют «небольшие» как менее 2 мм без значительного вовлечения стромы или расплавления. Пациентам низкого риска рекомендуется эмпирическое лечение моксифлоксацином 0,5% без консервантов. Многочисленные исследования показали, что фторхинолоны четвёртого поколения с их широким спектром активности в отношении грамположительных и грамотрицательных микроорганизмов сопоставимы по эффективности с фортифицированными антибиотиками. Видовая идентификация зависит от локализации практики и может не иметь значения у пациентов низкого риска. Однако в национальном масштабе и в серии случаев местной окружной больницы виды Staphylococcus становятся более резистентными к фторхинолонам. Поэтому важно ежедневное наблюдение даже у пациентов низкого риска для оценки улучшения. При отсутствии улучшения рекомендуется «лекарственные каникулы» и переход к алгоритму лечения высокого риска. Микробный кератит высокого риска: это крупные, угрожающие зрению, некротизирующие или лимбальные/склеральные поражения. Кроме того, пациенты с атипичными признаками (пушистые края, иммунокомпрометация, травма, применение кортикостероидов или не отвечающие на местные противомикробные препараты) также считаются группой высокого риска. Для подбора оптимального лечения в первую очередь проводятся окрашивание и посев. Окрашивание жизненно важно, так как обеспечивает почти немедленную идентификацию. Для стандартных случаев микробного кератита высокого риска предпочтительно использовать как грам-окрашивание, так и окрашивание акридиновым оранжевым ввиду их высокой специфичности. Пациенты с любым атипичным анамнезом или признаками должны быть обследованы на атипичную инфекцию при первичном соскобе. После окрашивания и посева пациентам высокого риска назначается эмпирическая терапия фортифицированными тобрамицином 14 мг/мл и ванкомицином от 10 до 25 мг/мл каждые 30 минут или каждые 2 часа в чередующемся режиме в зависимости от тяжести. Данная комбинация обеспечивает активность как против грамотрицательных, так и грамположительных микроорганизмов. Важно немедленно оценить результаты окрашивания, так как процесс занимает всего около 15–25 минут для почти мгновенной идентификации. Хотя некоторые учреждения (например, больницы и учебные центры) могут обрабатывать материал немедленно, большинство частных кабинетов вынуждены отправлять образцы в лабораторию, и результаты могут быть доступны только через 24 часа и более. Результаты посева на чувствительность следует отслеживать ежедневно, хотя рост большинства бактерий происходит в первые 24–48 часов. Если посевы оказались безрезультатными, а пациент всё ещё не улучшается на фоне эмпирической антибиотикотерапии, рассматриваются несколько причин: наиболее очевидная — несоблюдение режима лечения пациентом; другая возможность — полимикробная или резистентная инфекция, которая не лечится должным образом; последняя возможность — язва представляет собой не бактериальный кератит, а другой, возможно, атипичный возбудитель, ранее не рассматривавшийся. Из-за длительного характера и токсичности лечения атипичных инфекций роговицы обычно требуется подтверждение с помощью патогномоничного обследования, посева, патологии или амплификации нуклеиновых кислот (ПЦР) перед назначением противогрибковых, противовирусных или противоамёбных препаратов. Поэтому после «лекарственных каникул» повторно и расширенно проводится окрашивание, посев или ПЦР. Обычно 24-часовых «лекарственных каникул» достаточно. При риске неминуемого расплавления роговицы и дальнейшей потери зрения посев может быть выполнен без «лекарственных каникул». После второго отрицательного окрашивания и посева обычно выполняется биопсия роговицы при наличии достаточной толщины стромы для повторного культивирования, включая ПЦР. Конфокальная микроскопия является опцией для идентификации возбудителя, однако она известна своей зависимостью от оператора и может быть не столь патогномоничной, как молекулярные методы (например, ПЦР). Применение стероидов у пациентов с микробным кератитом высокого риска остаётся предметом частых дискуссий. Наиболее безопасным основанием для назначения стероидов является наличие подтверждённого посевом возбудителя, отвечающего на текущую антибактериальную терапию, но при этом бремя кератита велико с вовлечением центра. При рассмотрении возможности назначения стероидов сначала необходимо учесть противопоказания к применению кортикостероидов. Местные кортикостероиды могут ухудшать течение герпетического эпителиального, акантамёбного и грибкового кератита, а также приводить к задержке правильной диагностики и лечения. Не рекомендуется начинать стероиды, если текущая антибиотикотерапия неэффективна, поскольку микробный кератит может быть вызван атипичным возбудителем, состояние которого ухудшается на фоне стероидов. В субанализе исследования Steroids for Corneal Ulcers Trials (SCUT) у пациентов со зрением «счёт пальцев» или хуже и центральными язвами, вызванными высоковирулентными возбудителями, такими как Pseudomonas, было показано улучшение долгосрочного зрения при добавлении местных стероидов через 48 часов монотерапии местным моксифлоксацином. Дальнейший субанализ показал улучшение на одну строчку зрения, если стероиды начинали в течение 3 дней лечения, а не позже. Однако исследование SCUT не имело достаточной мощности для субанализа, и эти результаты следует рассматривать как рекомендации, а не абсолютные правила. Хотя исследования SCUT не выявили различий в долгосрочных исходах при добавлении местных кортикостероидов, следует отметить, что в исследовании стероиды начинали после подтверждения бактериального кератита посевом. В подгруппе случаев Nocardia в рамках SCUT кортикостероиды значительно ухудшали размеры рубцов и время заживления. Конечным вмешательством при микробном кератите высокого риска является терапевтическая сквозная кератопластика при угрожающей перфорации или при стойко незаживающих крупных язвах. Долгосрочные результаты кератопластики при активной инфекции вариабельны, поэтому она применяется как крайнее средство.