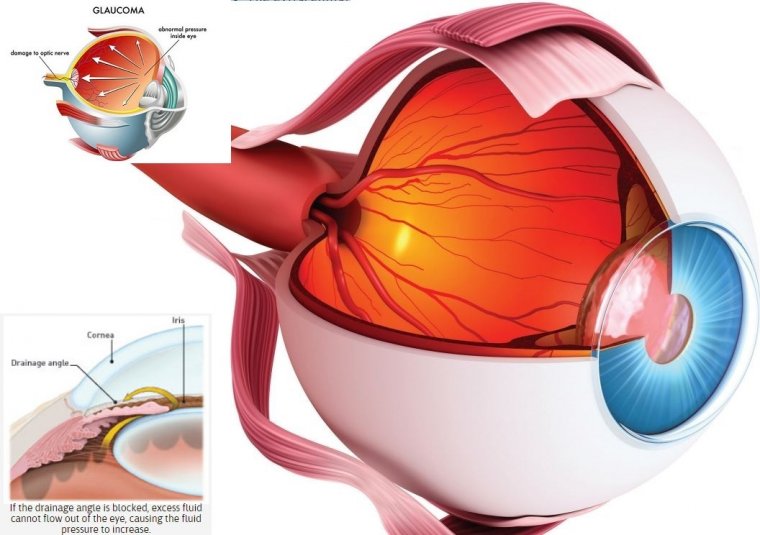
Причиной глаукомы может служить повышенное внутриглазное давление (ВГД), возникающее из-за неспособности глаза эффективно отводить жидкость. Прозрачная жидкость, называемая водянистой влагой, циркулирует в переднем сегменте глаза. Для поддержания постоянного здорового давления глаз непрерывно вырабатывает небольшое количество водянистой влаги, в то время как равный объем этой жидкости оттекает из глаза. Отток происходит через микроскопический канал — трабекулярную сеть (ТМ), сложную сеть клеток и тканей, расположенную в области угла передней камеры.
При глаукоме отток водянистой влаги через трабекулярную сеть нарушается. Если дренажная система становится менее эффективной (как при распространенной открытоугольной глаукоме), избыток жидкости не может правильно покинуть глаз, что приводит к повышению ВГД. Со временем повышенное давление вызывает повреждение нервных волокон. При полной блокаде дренажного угла давление растет быстро, развивается приступ закрытоугольной глаукомы с выраженной болью в глазу и брови, тошнотой и рвотой. Такое состояние требует неотложной медицинской помощи.
Пути вмешательства и патогенез заболевания
Исследователи изучают различные внутриглазные пути, чтобы определить, как воздействовать на механизмы развития болезни. Благодаря лучшему пониманию механизмов оттока и трабекулярной сети, пациентам с глаукомой в будущем может потребоваться менее частое наблюдение. Глаукома поражает трабекулярную сеть и зрительный нерв. Зона юкстаканаликулярной ткани (ЮКТ) в ТМ является анатомической областью, контролирующей сопротивление оттоку. Эта область не статична и постоянно подвергается ремоделированию.
В области ЮКТ выделяют два основных пути: параклеточный (между клетками) и трансклеточный (через клетки). Внеклеточный матрикс, на котором располагаются клетки и поддерживается их структура, является важным компонентом контроля ВГД. Увеличенное количество внеклеточного матрикса в ЮКТ — единственный известный фактор при первичной открытоугольной глаукоме (ПОУГ), который «забивает» поток жидкости через эту область. Многочисленные лекарственные препараты и хирургические вмешательства снижают ВГД, но не воздействуют на корень патологического процесса при глаукоме. Врачи снижают давление, изменяя физиологию, но не нарушая патофизиологию заболевания. По этой причине глаукома может прогрессировать, несмотря на снижение ВГД. Даже при отсутствии потери полей зрения пациенты нуждаются в постоянном наблюдении для контроля адекватности лечения.
Поразительная статистика: от 7% до 14% пациентов становятся юридически слепыми на один глаз в течение двух лет, несмотря на оптимальное лечение, поскольку первопричина глаукомы не устраняется медикаментами и хирургией.
Исследования трабекулярной сети и роль SPARC
Трансформирующий фактор роста бета-2 (TGF β2) признан важным фактором развития глаукомы. Его концентрация повышена до трех раз в водянистой влаге глаз с ПОУГ; TGF β2 также повышает ВГД в перфузируемых донорских передних сегментах человека и вызывает изменения во внеклеточном матриксе ЮКТ, сходные с глаукоматозными. TGF β2 повышает ВГД у живых мышей и крыс и вызывает повреждение зрительного нерва. Исследователи предполагают, что всё, что контролирует внеклеточный матрикс, имеет значение для регуляции ВГД. Матриклеточные белки позволяют клеткам управлять окружающим внеклеточным матриксом. Ученые изучили семейство таких белков и обнаружили три: SPARC, тромбоспондин-1 и -2, которые снижают ВГД у мышей с удаленными соответствующими генами.
Более детальное изучение SPARC показало, что он является одним из наиболее активно транскрибируемых генов в ТМ; он обнаруживается по всей ТМ и в высокой концентрации — в ЮКТ. И, что важно, SPARC — один из наиболее активно секретируемых белков в ответ на TGF β2 и повышение ВГД. Было высказано предположение, что повышение ВГД зависит от SPARC. Ключевое открытие: при введении TGF β2 нормальным мышам ВГД повышалось. Однако у мышей, не способных секретировать SPARC, TGF β2 не вызывал повышения ВГД. Это неожиданное и крайне важное открытие стало «Святым Граалем» глаукомы.
Белок SPARC — один из немногих белков, регулирующих ВГД. Исследователи начинают раскрывать эти пути в надежде воздействовать на них и тем самым прервать патофизиологию заболевания. Главный вывод: был обнаружен белок, который в норме регулирует ВГД и, вероятно, имеет критическое значение для патофизиологии ПОУГ. Это открытие в конечном итоге позволит вмешиваться в процесс на молекулярном уровне.