В медицинской литературе описаны два типа дефицита плазминогена. Врожденный дефицит плазминогена 1-го типа представляет собой количественное нарушение с параллельным снижением уровня иммунореактивного и функционального плазминогена; данный тип также называется гипоплазминогенемией, является тяжелым заболеванием и составляет основное содержание настоящего отчета.
Врожденный дефицит плазминогена 2-го типа является качественным дефицитом с нормальным или почти нормальным уровнем иммунореактивного плазминогена при сниженной активности и также называется дисплазминогенемией; дефицит плазминогена 2-го типа не ассоциирован с развитием псевдомембран и поэтому не рассматривается.
Врожденный дефицит плазминогена — это заболевание, которое приводит к воспалительным разрастаниям на слизистых оболочках — влажных тканях, выстилающих отверстия тела, такие как веки и внутренняя поверхность рта.
Развитие разрастаний обычно провоцируется инфекциями или травмами, но они также могут возникать спонтанно при отсутствии известных триггеров. После удаления разрастания могут рецидивировать.
Врожденный дефицит плазминогена чаще всего поражает конъюнктиву — слизистую оболочку, защищающую белочную оболочку глаза (склеру) и выстилающую веки.
Характерным признаком этого заболевания является лигвинозный конъюнктивит, при котором накопление белка фибрина вызывает воспаление конъюнктивы и приводит к образованию толстых, деревянистых (лигвинозных), воспаленных разрастаний желтого, белого или красного цвета. Лигвинозный конъюнктивит чаще всего возникает на внутренней поверхности век.
Однако примерно в одной трети случаев лигвинозный конъюнктивит над склерой распространяется на роговицу — прозрачную оболочку, защищающую радужку и зрачок. Такие разрастания могут приводить к разрывам роговицы или вызывать рубцевание. Данные проблемы с роговицей, а также обструкция разрастаниями внутри века могут привести к потере зрения.
У людей с врожденным дефицитом плазминогена также могут развиваться лигвинозные разрастания на других слизистых оболочках, включая внутреннюю поверхность рта и десны, слизистую оболочку носовой полости, а у женщин — влагалища.
Разрастания на слизистых оболочках желудочно-кишечного тракта могут приводить к образованию язв. Разрастания также могут развиваться в трахее, что вызывает угрожающую жизни обструкцию дыхательных путей, особенно у детей.
В небольшом числе случаев у пораженных лиц с рождения нарушен отток жидкости, окружающей и защищающей головной и спинной мозг (цереброспинальной жидкости), что приводит к накоплению этой жидкости в черепе (окклюзионная гидроцефалия). Неясно, как этот признак связан с другими проявлениями врожденного дефицита плазминогена.
При отсутствии лечения
При отсутствии лечения лигвинозный конъюнктивит может привести к нарушению зрения или слепоте. Появление зрительных симптомов обычно приводит к тому, что офтальмологи становятся первыми клиницистами, оценивающими состояние пациентов и потенциально устанавливающими диагноз на момент возникновения симптомов.
Поскольку распространенность заболевания в настоящее время оценивается в 1–2 случая на миллион в общей популяции, врожденный дефицит плазминогена часто диагностируется неправильно. Это связано как с его редкостью, так и с тем, что симптомы часто приписываются другим, более распространенным заболеваниям.
Существуют важные пробелы в знаниях о врожденном дефиците плазминогена: мало известно об его истинной заболеваемости, триггерах, течении болезни в зависимости от установленных категорий тяжести и общем влиянии.
Ограничена количественная информация о ведении заболевания, необходимости наблюдения за другими потенциально пораженными областями, бремени болезни и опыте пациентов.
Клиницисты в настоящее время полагаются на anecdotal информацию, личный опыт и ограниченное число клинических наблюдений для разработки планов лечения пациентов.
На момент публикации не существовало зарегистрированной специфической и эффективной терапии для лечения врожденного дефицита плазминогена, что усугубляло пробелы в знаниях и способствовало неоптимальным результатам.
Команды из Indiana Hemophilia and Thrombosis Center (IHTC), Fondazione Angelo Bianchi Bonomi, IRCCS Ca Granda Ospedale Maggiore Policlinico of Milan (IRCCS) и University of Milan (UNIMI) работали над решением этих проблем в рамках первого совместного исследования естественного течения врожденного дефицита плазминогена под названием Hypoplasminogenemia: An International RetroSpecTive and PrOspective CohorRt StudY (HISTORY).
Результаты этого исследовательского проекта могли иметь важные последствия для офтальмологов в будущем.
Текущий сбор данных о нарушениях свертываемости крови
Существовало два основных репозитория данных о пациентах с редкими нарушениями свертываемости крови, которые вели American Thrombosis and Hemostasis Network (ATHN) и European Network of Rare Bleeding Disorders (EN-RBD).
Хотя эти организации добились больших успехов в сборе данных, несколько проблем ограничивали их применимость. Ни одна из программ специально не рассматривала врожденный дефицит плазминогена.
ATHN совместно с Centers for Disease Control накопила репозиторий данных с более чем 80 000 участников, но это была программа, базирующаяся в США, что делало данные о лечении и исходах включенных популяций менее применимыми к пациентам, живущим в других странах с иными медицинскими ресурсами и популяциями.
EN-RBD создала Rare Bleeding Disorders Database в 2004 году для систематизации клинических, генетических данных и данных о лечении редких нарушений свертываемости крови, отличных от классической гемофилии A и B. Ранние данные исследования были собраны от 592 пациентов из 11 европейских стран.
Эти данные позволили разработать новую систему классификации тяжести симптомов кровотечения, связанных с этими нарушениями.
С момента создания база данных (позже переименованная в Prospective Rare Bleeding Disorders Database (PRO-RBDD)) расширилась и включила проспективный сбор данных от пациентов из 62 центров по всему миру.
Целью расширенного исследования была поддержка более точной оценки распространенности конкретных редких нарушений свертываемости крови, а также получение новых сведений о симптомах, бремени болезни и клиническом ведении.
Хотя результаты могли предоставить важную информацию, касающуюся всех редких нарушений свертываемости крови, исследование не включало врожденный дефицит плазминогена.
Создание проекта HISTORY
Проект HISTORY стал первым международным исследованием, направленным на оценку и определение естественного течения врожденного дефицита плазминогена. Исследователи в области гематологии из Blood Ties приступили к первому в мире совместному исследованию естественного течения врожденного дефицита плазминогена, и офтальмологам предстояло сыграть решающую роль в определении категорий тяжести и выявлении триггеров клинических проявлений заболевания.
Координируемый IHTC и IRCCS/UNIMI, проект являлся расширением PRO-RBDD и должен был длиться четыре года: участники предоставляли ретроспективные данные за один год на исходном уровне, после чего следовали три года проспективных данных.
При включении в исследование субъекты проходили очную оценку в исследовательском центре для сбора ретроспективных данных, физикального обследования и получения биологических образцов. Затем сбор данных последующего наблюдения проводился по телефону каждые шесть месяцев до окончания исследования, когда участников осматривали очно.
Если у субъектов возникало клиническое событие, предположительно связанное с развитием псевдомембран, или другое медицинское событие, например беременность, их осматривали очно для оценки и сбора образцов.
Исследователи планировали собрать данные примерно от 500 участников, включая до 100 пациентов с врожденным дефицитом плазминогена и их родственников первой степени родства.
Исследование должно было оценить несколько параметров, включая общее состояние здоровья участников, возраст на момент диагностики, причину первоначального скрининга на врожденный дефицит плазминогена, фенотипы и генотипы.
Участники с подтвержденным диагнозом врожденного дефицита плазминогена классифицировались как бессимптомные, интермиттирующе симптомные или постоянно симптомные, и их данные рассматривались с учетом пола, факторов окружающей среды, генетической информации и других лабораторных показателей.
Поражения, связанные с врожденным дефицитом плазминогена, наблюдались по локализации, частоте и продолжительности, а также по типу и длительности лечения.
Исследование должно было оценить лабораторные параметры, информацию о ведении хирургических процедур, акушерские данные и любые осложнения лечения. Ключевым аспектом этого исследования стал сбор данных от бессимптомных родственников пациентов с врожденным дефицитом плазминогена первой степени родства.
Эти данные могли внести значительный вклад в литературу о врожденном дефиците плазминогена, поскольку бессимптомные пораженные пациенты могли не тестироваться на заболевание, а гетерозиготные лица не проходили рутинную оценку или наблюдение.
Данные от бессимптомных участников исследования могли содержать ценную информацию о триггерах клинических проявлений заболевания. Кроме того, данные от гетерозиготных членов семей могли дать представление о взаимосвязи между минимальным уровнем активности плазминогена и естественным течением врожденного дефицита плазминогена.
Значение исследования врожденного дефицита плазминогена для офтальмологии
Исследователи надеялись использовать данные и образцы для устранения пробелов в знаниях о клиническом ведении врожденного дефицита плазминогена, в конечном итоге установив более высокий стандарт медицинской помощи.
Учитывая, что лигвинозный конъюнктивит является частым первым симптомом врожденного дефицита плазминогена, данные могли оказать существенную поддержку офтальмологам и другим медицинским работникам, занимающимся заболеваниями глаз, которые в то время располагали очень ограниченной информацией и рекомендациями по ведению этих пациентов.
Например, если у пациента развивался лигвинозный конъюнктивит, не существовало данных для оценки вероятности развития поражений в других системах, включая жизнеугрожающие, а также не было ясно, какие методы наблюдения следует использовать и когда, как часто следует наблюдать каждого человека и как долго следует проводить лечение.
Хотя офтальмолог мог обеспечить некоторое облегчение симптомов при лигвинозном конъюнктивите, он не мог предсказать, каких других специалистов потребуется посетить пациенту.
Исследование HISTORY могло поддержать разработку последовательных и эффективных стандартов медицинской помощи для пациентов с врожденным дефицитом плазминогена, включая тех, у кого развился лигвинозный конъюнктивит.
На момент публикации не существовало одобренной терапии врожденного дефицита плазминогена, поэтому лекарства назначались не по инструкции, что приводило к неоднородным и неоптимальным результатам.
Проект HISTORY был направлен на сбор данных таким образом, чтобы позволить разработать и подтвердить категории тяжести заболевания, более точно прогнозировать течение болезни, эффективно определять конкретные потребности в наблюдении у подгрупп пациентов, создавать алгоритмы лечения, более полные рекомендации и лучшие практики для ведения заболевания.
Проект HISTORY также мог помочь создать основу для будущих клинических исследований посредством разработки биорепозитория и использования расширенных методов исследования свертываемости крови. Исследователи могли потенциально использовать информацию, собранную в ходе исследования, для оценки использования локально проводимых тестов в качестве диагностических инструментов.
Разработка специфического для заболевания скринингового теста позволила бы помочь в диагностике и прогнозировании течения болезни, облегчая раннее вмешательство и установление более точной распространенности.
На момент публикации диагноз врожденного дефицита плазминогена подтверждался анализом активности плазминогена и уровня антигенов в крови. Эти тесты были не universally доступны и могли не быть стандартизированы. Анализ мутаций обеспечивал дополнительное подтверждение, но также был доступен не всегда.
Клинические исследования ультраредких заболеваний, на примере врожденного дефицита плазминогена, сталкивались с трудностями в идентификации пациентов, фенотипической гетерогенности и, в конечном счете, в наборе участников. Малочисленность пораженных лиц, участвующих в испытаниях, затрудняла обобщение данных.
Данные, собранные и проанализированные в ходе этого исследования, могли помочь в отборе пациентов для будущих клинических испытаний.
Хотя на тот момент не существовало одобренных специфических и эффективных методов лечения, исследователи изучали использование концентрата плазминогена, выделенного и очищенного из крови здоровых доноров, для лечения врожденного дефицита плазминогена. Исследуемая терапия находилась на рассмотрении FDA.
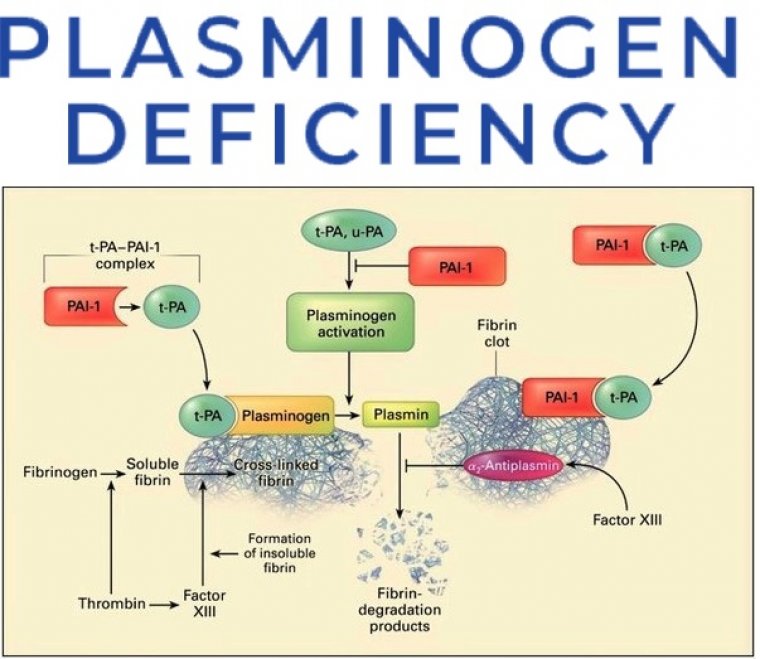
Плазминоген является ключевым зимогеном, играющим фундаментальную роль как предшественник плазмина — основного фермента, участвующего в лизисe тромбов и клиренсе фибрина; таким образом, плазминоген играет центральную роль в поддержании слизистых оболочек, заживлении ран, миграции клеток, ремоделировании тканей, ангиогенезе и эмбриогенезе.
Одной из важнейших целей проекта HISTORY было повышение осведомленности о врожденном дефиците плазминогена среди офтальмологов и других медицинских специалистов, которые могли играть центральную роль в ведении пациентов. Предоставление офтальмологам нового уровня количественной информации и понимания врожденного дефицита плазминогена могло улучшить время постановки диагноза и способность направлять пациентов на надлежащую медицинскую помощь.