Исследовательская группа из Калифорнийского университета в Ирвайне (University of California, Irvine) сообщила об открытии уникального антитела, способного подавить ключевой механизм развития пигментного ретинита (Retinitis Pigmentosa). Данное заболевание приводит к дегенерации центрального, сумеречного и цветового зрения.
Публикация о взаимодействии родопсина с наноантителом
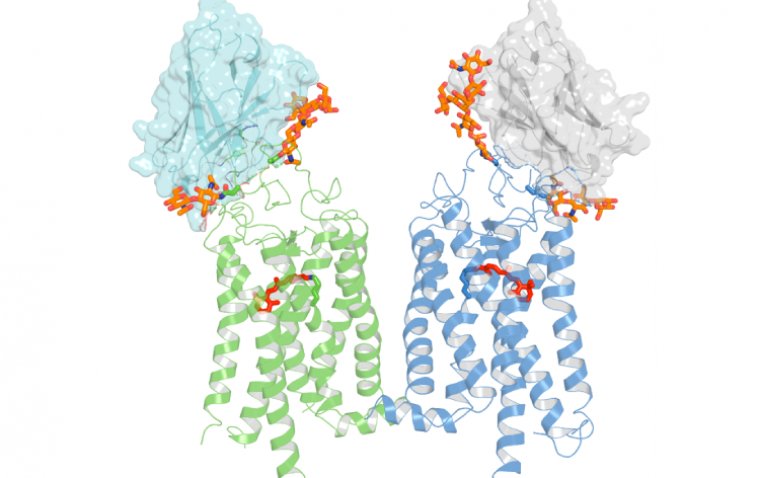
Научная работа под названием «Structural basis for the allosteric modulation of rhodopsin by nanobody binding to its extracellular domain» («Структурная основа аллостерической модуляции родопсина при связывании наноантитела с его внеклеточным доменом») была опубликована в журнале Nature Communications. Среди авторов — Ар У, PhD, Дэвид Салом, PhD, Джон Д. Хонг, Александер Творак, PhD, Филип Д. Кайзер, PharmD, PhD, Кшиштоф Пальчевски, PhD. Работа выполнена на базе кафедры офтальмологии Института глаза им. Гэвина Герберта при Калифорнийском университете в Ирвайне. В исследовании также принял участие Джей Стейарт, PhD, из Свободного университета Брюсселя (Vrije Universiteit Brussel, VUB).
Что такое пигментный ретинит?
Пигментный ретинит (RP) — группа наследственных заболеваний сетчатки, расположенной в заднем отделе глаза. Патология обусловлена гибелью фоторецепторных клеток, воспринимающих световые сигналы. На сегодняшний день этиотропного лечения RP не существует, и разработка новых методов терапии опирается на клеточные и генные технологии.
Фокус на родопсин-ассоциированную аутосомно-доминантную форму RP (adRP)
Ученые UCI сосредоточили усилия на молекуле родопсина, ключевом светочувствительном белке сетчатки человека, локализованном в палочковых фоторецепторах. Мутации в гене родопсина служат основной причиной adRP. Более 150 мутаций в этом гене способны вызывать пигментный ретинит, что существенно затрудняет разработку таргетной генной терапии, пояснил Кшиштоф Пальчевски, PhD, профессор Медицинской школы UCI. Однако высокая распространенность RP стимулирует значительные инвестиции в поиск новых методов лечения.
Несмотря на столетие изучения родопсина, многие детали его работы по преобразованию света в клеточный сигнал оставались труднодоступными для эмпирического анализа. В данном исследовании ученые применили особый тип антител, получаемых от лам, — так называемое наноантитело (nanobody). Этот белок способен блокировать процесс фотоактивации родопсина, позволяя детально изучить его структуру с высоким разрешением.
Команда разработала наноантитела, действующие по новому механизму. Эти агенты обладают высокой специфичностью и распознают родопсин с внеклеточной стороны, что позволяет «заблокировать» этот GPCR-рецептор в несигнализирующем состоянии, сообщил Дэвид Салом, PhD, научный сотрудник Медицинской школы UCI.
Было сделано интригующее открытие: наноантитела связываются с неожиданным участком молекулы родопсина, расположенным вблизи зоны присоединения ретиналя. Кроме того, стабилизирующее действие этих наноантител распространяется и на мутантные формы родопсина, ассоциированные с заболеваниями сетчатки, что указывает на их терапевтический потенциал.
В будущем планируется заняться направленной эволюцией полученных наноантител in vitro, а также оценить безопасность и эффективность наноантительной генной терапии для лечения RP, отметила Ар У, PhD, научный сотрудник Медицинской школы UCI.
Продвижение доклинических исследований наноантител
Исследователи намерены повысить способность наноантител различать родопсин разных видов, в том числе мышиный, для использования многочисленных доклинических моделей adRP. Также планируется применить эти наноантитела для решения давней задачи структурной биологии — расшифровки фундаментальных промежуточных состояний родопсина в переходе от покоящейся формы к полностью активированной лигандом.
Источник
https://medschool.uci.edu/news/uc-irvine-researchers-discover-nanobody-which-may-lead-treatment-retinitis-pigmentosa