Меланома увеального тракта (радужки, цилиарного тела и хориоидеи), несмотря на свою редкость, является наиболее распространенным первичным внутриглазным злокачественным новообразованием у взрослых. Средний возраст-скорректированный показатель заболеваемости увеальной меланомой в Соединенных Штатах составлял приблизительно 4,3 новых случая на миллион человек, при этом четких различий в зависимости от широты не наблюдалось. У мужчин заболеваемость была выше (4,9 случая на миллион), чем у женщин (3,7 случая на миллион). Возраст-скорректированная заболеваемость этой опухолью оставалась стабильной по крайней мере с начала 1970-х годов. Показатели заболеваемости в США были низкими по сравнению с данными других стран, которые варьировались от 5,3 до 10,9 случая на миллион. Часть этих различий могла быть обусловлена неодинаковыми критериями включения и методами расчета. Увеальная меланома диагностировалась преимущественно в пожилом возрасте, с прогрессивно повышающимся возраст-специфическим показателем заболеваемости, достигающим пика около 70 лет.
Окулярная меланома (ОМ) являлась наиболее распространенным первичным раком глаза у взрослых. Чаще всего она встречалась у светлопигментированных людей со средним возрастом 55 лет, хотя могла развиться у представителей любой расы и в любом возрасте. ОМ представляла собой злокачественную опухоль, способную расти и метастазировать в другие части тела — этот процесс, известный как метастазирование, часто заканчивался летально и наблюдался примерно в половине случаев. Несмотря на происхождение из одних и тех же клеток — меланоцитов, — ОМ отличалась от кожной меланомы и не была связана с воздействием солнечного излучения. Окулярная меланома занимала второе место по распространенности среди всех типов меланомы после кожной, составляя около 5% от всех меланом.
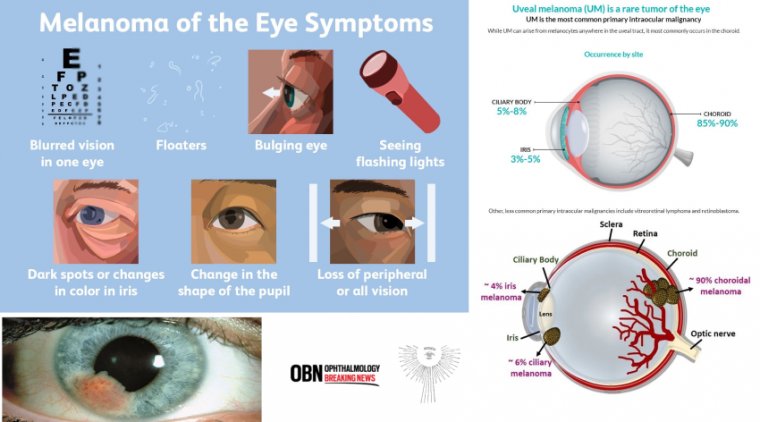
Подобно меланоме кожи, ОМ была малоизученным и «тихим» убийцей. В большинстве случаев окулярная меланома развивалась медленно из пигментных клеток хориоидеи (хориоидальная меланома), но также могла возникать из пигментных клеток радужки и цилиарного тела. ОМ также называли увеальной меланомой, поскольку увеальный тракт является частью глаза, содержащей две области, где ОМ может возникать обычно. ОМ представляла собой агрессивную форму рака, которая могла поражать любую из трех областей глаза: радужку, цилиарное тело и/или хориоидею (сосудистую оболочку между сетчаткой и склерой). Эти три области в совокупности известны как увеа или увеальный тракт, и ОМ могла возникнуть в любой их комбинации. Меланомы радужки имели наилучший прогноз, тогда как меланомы цилиарного тела — наихудший. Большинство увеальных меланом происходили из хориоидеи; цилиарное тело было менее частым местом возникновения, а радужка — самым редким. Меланома также могла возникнуть в тонкой выстилке над белой частью глаза (конъюнктиве) или на веке, но это было очень редким явлением.
Было известно, что воздействие ультрафиолетовых лучей повышает риск развития меланомы кожи. Люди с легко обгорающей кожей — светлокожие, со светлыми или рыжими волосами и голубыми глазами — были в группе наибольшего риска. Однако убедительных доказательств связи ультрафиолетового облучения с ОМ не существовало.
Эми К. Шефлер (Amy C. Schefler), доктор медицины, из Retina Consultants of Houston, сообщила, что светоактивируемый препарат AU-011 обладал потенциалом стать первой таргетной терапией, когда-либо разработанной для первичного лечения окулярной меланомы. По данным компании Aura Biosciences, разработавшей эту светоактивируемую технологию, пациенты с диагнозом окулярной меланомы сталкивались с ограниченным выбором неэффективных вариантов лечения, которые часто приводили к тяжелой потере зрения, удалению глаза и, примерно в половине случаев, к метастазированию в печень, где заболевание почти всегда заканчивалось летально.
Доктор Шефлер пояснила, что AU-011 является первым в своем классе таргетным препаратом — новым конъюгатом белкового капсида и красителя, рекомбинантно полученным из белков капсида вируса папилломы. FDA уже присвоило ему статусы «Ускоренный процесс разработки» (Fast Track Designation) и «Орфанный препарат» (Orphan Drug Designation), признав отсутствие одобренных FDA методов лечения и серьезный, угрожающий жизни характер заболевания.
Механизм действия AU-011 заключался в targeted acute tumor cellular necrosis upon light activation. Конъюгаты капсида доставлялись интравитреальной инъекцией и селективно связывались с опухолевыми клетками хориоидеи, не затрагивая сетчатку и другие ключевые структуры глаза. Эта уникальная селективность обусловлена связыванием конъюгатов капсида с модифицированными гепарансульфат-протеогликанами, экспрессируемыми на поверхности опухолевых клеток. Белок капсида был конъюгирован с мощным фотосенсибилизатором фталоцианином — IRDye 700DX, который оказывал цитотоксическое действие на опухоль при активации светом от ближнего инфракрасного лазера с длиной волны 689 нм.
Доктор Шефлер отметила, что механизм действия обладал двойной селективностью: во-первых, конъюгаты капсида связывались исключительно с опухолевыми клетками, а во-вторых, луч лазера активировал конъюгированный краситель только внутри опухоли, генерируя мощные цитотоксические свободные радикалы кислорода, которые нарушали мембрану опухолевой клетки, приводя к таргетному и острому некрозу опухолевых клеток.
В доклинических исследованиях на кроликах с окулярными опухолями животные получали лечение дважды в неделю светоактивируемым AU-011 на 1-й и 8-й дни. Результаты продемонстрировали полный некроз опухолей, имплантированных в хориоидею, без повреждения прилегающей сетчатки, даже для опухолей толщиной более 10 мм. Данные на животных показали дозозависимый эффект: с увеличением дозы препарата некроз опухоли возрастал, в то время как сетчатка и другие здоровые ткани не страдали. Сила этих доклинических данных позволила получить статус «Орфанного препарата» от FDA в 2015 году. Доктор Шефлер представила промежуточные 6-месячные результаты по AU-011.
Дизайн исследования
Доктор Шефлер сообщила, что исследование фазы Ib/II представляло собой 2-летнее, проспективное, многоцентровое открытое исследование с когортами однократной и многократной повышающейся дозы. Три пациента с хориоидальной меланомой получили однократное интравитреальное введение конъюгата капсида на каждом из трех субтерапевтических уровней повышающейся дозы (20 мкг, 40 мкг или 80 мкг) с последующей светоактивацией лазером 689 нм с флюенсом 50 Дж/см². Фаза многократной повышающейся дозы состояла из четырех дополнительных когорт по три пациента в каждой. В каждой когорте количество интравитреальных введений было увеличено до трех еженедельных процедур, а количество лазерных активаций — до двух аппликаций в тот же день с интервалом 30 минут. Целью фазы MAD было определение максимально переносимой дозы и режима для клинических исследований фазы III. Первичной целью исследования была безопасность, вторичные исходы включали эффективность и иммуногенность.
Результаты исследования на текущий момент
Доктор Шефлер сообщила, что на тот момент было пролечено 22 пациента: девять в когорте однократной повышающейся дозы и 13 в когорте многократной повышающейся дозы. Серьезных нежелательных явлений, связанных с лечением, или тяжелых нежелательных явлений зарегистрировано не было. Дозолимитирующей токсичности не наблюдалось. Нежелательные явления поддавались контролю с помощью стандартных методов лечения и не имели дальнейших клинических последствий. Острота зрения до лечения сохранилась у всех субъектов, наблюдавшихся в течение 6–12 месяцев. Все нежелательные явления были расценены как легкие или умеренные и включали переднее или заднее воспаление (у 10 и 11 пациентов соответственно), которое начиналось примерно через 4 недели после лечения. У 6 из 18 пациентов отмечалось транзиторное повышение внутриглазного давления.
Доктор Шефлер отметила, что воспаление и повышение ВГД на тот момент поддавались контролю с помощью стандартного лечения и разрешались без клинических последствий. Интересно, что воспаление являлось ожидаемым ответом на механизм действия AU-011 в результате острого некроза опухолевых клеток и могло быть даже полезным с точки зрения формирования опухоль-специфического Т-клеточного иммунного ответа. При фундоскопической оценке пациентов после лечения было видно, что заднее воспаление, по-видимому, начиналось в опухоли и, вероятно, было связано с некрозом опухоли.
Доктор Шефлер сообщила, что практически не было изменений остроты зрения (все пациенты, наблюдавшиеся в течение 6 месяцев и более, были в пределах одной буквы от исходного уровня), независимо от локализации опухоли, включая те, которые находились прямо в центре фовеа или касались зрительного нерва. В трех когортах однократной дозы у нескольких пациентов наблюдалось стабильное заболевание через 12 месяцев, даже несмотря на то, что это считалось субтерапевтической дозой. В когортах многократной дозы у всех пациентов сохранялось стабильное заболевание при последующем наблюдении, а у ряда пациентов отмечалось уменьшение опухоли, измеренное с помощью ультразвука.
Доктор Шефлер пояснила, что исследователи измеряли рост опухоли, предполагая, что при отсутствии дальнейшего роста опухоль подвергается некрозу и больше не обладает злокачественным потенциалом. Конечно, наблюдение уменьшения опухоли и воспаления вокруг нее на ранних сроках было обнадеживающим для подтверждения биологической активности препарата, но наиболее важным показателем эффективности было отсутствие дальнейшего роста опухоли при длительном наблюдении с хорошим сохранением зрения.