FDA
Статьи с этим тегом
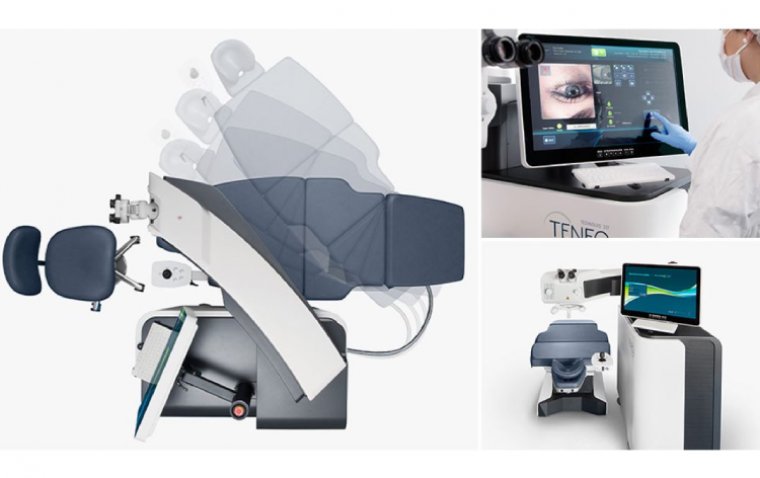
FDA одобрила эксимерную лазерную платформу Teneo производства Bausch + Lomb
FDA одобрило эксимерную лазерную платформу Teneo от Bausch + Lomb для LASIK-коррекции миопии и миопического астигматизма. Устройство отличается высокой частотой айтрекинга (1740 Гц), компактностью и трехшаговым интерфейсом управления.
Читать далее →
FDA одобрило глазные капли с клобетазолом для купирования воспаления и боли после операций на глазах
FDA одобрило клобетазола пропионат (APP13007) для лечения послеоперационного воспаления и боли после офтальмологических операций. Препарат на основе наночастиц APNT требует закапывания дважды в день в течение 14 дней без снижения …
Читать далее →
Препарат NT-501 компании Neurotech Pharmaceuticals получил статус приоритетного рассмотрения FDA при лечении макулярной телеангиэктазии 2 типа
FDA присвоило статус приоритетного рассмотрения заявке Neurotech Pharmaceuticals на препарат NT-501 для лечения макулярной телеангиэктазии 2 типа. Решение ожидается в течение 6 месяцев, целевая дата по PDUFA — 17 декабря …
Читать далее →
Компания Ocugen инициировала фазу 3 клинического исследования генной терапии OCU400 при пигментном ретините
Компания Ocugen инициировала фазу 3 клинического исследования liMeliGhT для генной терапии OCU400 при пигментном ретините после введения первой дозы первому пациенту. Исследование основано на обнадеживающих данных фазы 1/2 и направлено …
Читать далее →
FDA разрешила Ocugen начало ключевого исследования фазы 3 по генной терапии пигментного ретинита
FDA разрешило Ocugen начало фазы 3 клинического исследования OCU400 — первой широкопоказанной генной терапии пигментного ретинита. Исследование включит 150 пациентов, в том числе с мутацией RHO и независимо от мутации, …
Читать далее →
Компания Glaukos получила постоянный J-код для внутрикамерного импланта iDose TR
Компания Glaukos получила постоянный J-код (J7355) от CMS для внутрикамерного импланта iDose TR с травопаростом 75 мкг, применяемого при открытоугольной глаукоме и офтальмогипертензии. Код вступил в силу 1 июля 2024 …
Читать далее →
FDA одобрило IND-заявку Ascidian Therapeutics на препарат ACDN-01 для лечения болезни Штаргардта
FDA одобрило IND-заявку Ascidian Therapeutics на препарат ACDN-01 — первый в мире клинический редактор РНК-экзонов для лечения болезни Штаргардта. Компания планирует начать набор пациентов в исследование STELLAR фазы 1/2 в …
Читать далее →
AAO предостерегает от хирургических методов изменения цвета глаз
В феврале 2024 года Американская академия офтальмологии опубликовала предупреждение о рисках двух хирургических методов изменения цвета глаз — имплантации радужки и кератопигментации. В числе осложнений — слепота, глаукома, катаракта и …
Читать далее →
jCyte выводит терапию jCell в ключевое исследование в США при пигментном ретините
Компания jCyte, Inc. сообщила о переходе к ключевому исследованию фазы 2/3 терапии jCell при пигментном ретините в США после одобрения дизайна испытания FDA. Набор пациентов планируется начать во второй половине …
Читать далее →
FDA присвоила системе FYSX™ для регулирования офтальмотонуса классификацию De Novo
Компания Balance Ophthalmics получила классификацию De Novo от FDA для системы FYSX™ — первого немедикаментозного нехирургического метода лечения открытоугольной глаукомы и глаукомы нормального давления с использованием физических принципов для снижения …
Читать далее →
Pantheon Vision сообщает о прогрессе в разработке биоинженерных роговичных имплантатов по итогам встречи с FDA
Pantheon Vision успешно провела третью встречу с FDA по разработке биоинженерных имплантатов роговицы для лечения слепоты, от которой страдают 13 млн человек.
Читать далее →
FDA присвоила статус «Ускоренного рассмотрения» препарату NPI-001 компании Nacuity для терапии пигментного ретинита
FDA присвоило статус ускоренного рассмотрения препарату NPI-001 компании Nacuity для лечения пигментного ретинита, ранее препарат получил статус орфанного.
Читать далее →