FDA
Статьи с этим тегом

FDA одобрила двукратное суточное применение Vuity для лечения пресбиопии
FDA одобрило двукратное суточное применение раствора Vuity 1,25% для лечения пресбиопии у взрослых. Решение основано на результатах фазы 3 VIRGO, показавшей эффективность до 9 часов. Препарат принадлежит AbbVie (Allergan).
Читать далее →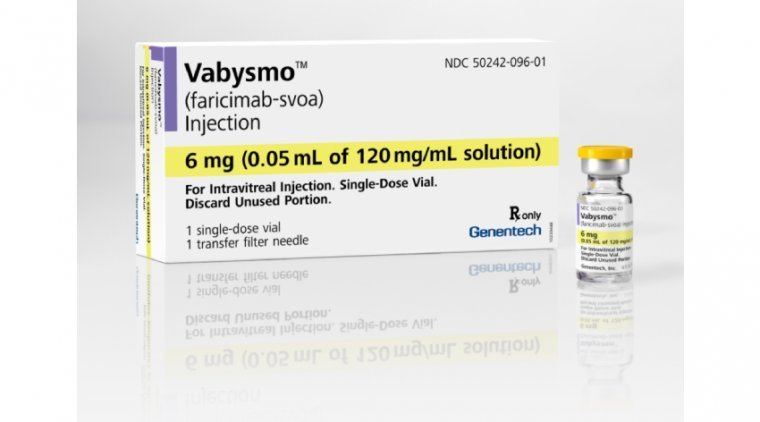
FDA одобрила к рассмотрению заявку на расширение показаний препарата Vabysmo (Genentech) при окклюзии вен сетчатки
В мае 2023 года FDA приняло к рассмотрению заявку Genentech на расширение показаний препарата Vabysmo (faricimab-svoa) для лечения макулярного отека вследствие окклюзии вен сетчатки на основании данных исследований BALATON и …
Читать далее →
Norlase привлек $11 млн на ускоренный выпуск лазерной системы ECHO Pattern
Norlase привлекла $11 млн в рамках крупнейшего инвестиционного раунда. Средства пойдут на ускоренный выпуск портативного паттернного лазера ECHO Pattern, недавно получившего одобрение FDA и CE Mark. Раунд возглавила West Hill …
Читать далее →
Компания Harrow приобрела права на Vevye в США и Канаде у Novaliq
В июле 2023 года Harrow приобрела права на Vevye (циклоспорин 0,1%) в США и Канаде у Novaliq. Препарат, одобренный FDA, стал первым раствором циклоспорина с эффективностью через 4 недели при …
Читать далее →
Обзор ключевых событий офтальмологической индустрии: декабрь 2025 г.
Дайджест новостей офтальмологии за декабрь 2025 г.: результаты Aviceda, разрешение FDA для EndoArt, первый пациент ViaLase, одобрение Byooviz в Европе, заявка на VIZZ в Южной Корее, патент Kiora, успех Belite …
Читать далее →
Обзор 2023 года: 15 ключевых прорывов в офтальмологии, случившихся впервые
Обзор 15 ключевых прорывов 2023 года в офтальмологии: от первой трансплантации целого глаза и лица до имплантации «умной» ИОЛ, диагностирующей болезнь Альцгеймера, и 5G-хирургии с расстояния 600 км.
Читать далее →
FDA санкционировала клинические испытания препарата AVD-104 компании Aviceda для лечения географической атрофии на фоне возрастной макулярной дегенерации
FDA одобрило заявку IND компании Aviceda Therapeutics на препарат AVD-104 для лечения географической атрофии при возрастной макулярной дегенерации, что позволило начать фазу 2 клинических исследований SIGLEC во втором квартале 2023 …
Читать далее →
FDA запросила дополнительное исследование репроxалапа компании Aldeyra Therapeutics при синдроме сухого глаза
В ноябре 2023 года Aldeyra Therapeutics получила от FDA письмо с полным ответом на заявку на репроxалап для лечения синдрома сухого глаза. Регулятор не выявил проблем с безопасностью, но запросил …
Читать далее →
Ocular Therapeutix получила одобрение FDA на модифицированное клиническое исследование Axpaxli при влажной форме ВМД
FDA одобрило модификацию протокола исследования SOL фазы 3 для имплантата Axpaxli (OTX-TKI) компании Ocular Therapeutix. Изменения направлены на ускорение набора пациентов с влажной формой ВМД и включают использование оптимизированного имплантата …
Читать далее →
Outlook Therapeutics получила одобрение FDA и финансирование для клинического исследования ONS-5010
Outlook Therapeutics в январе 2024 года получила письменное согласие FDA в рамках SPA для исследования NORSE EIGHT по препарату ONS-5010 при влажной ВМД и привлекла до $172 млн от инвесторов …
Читать далее →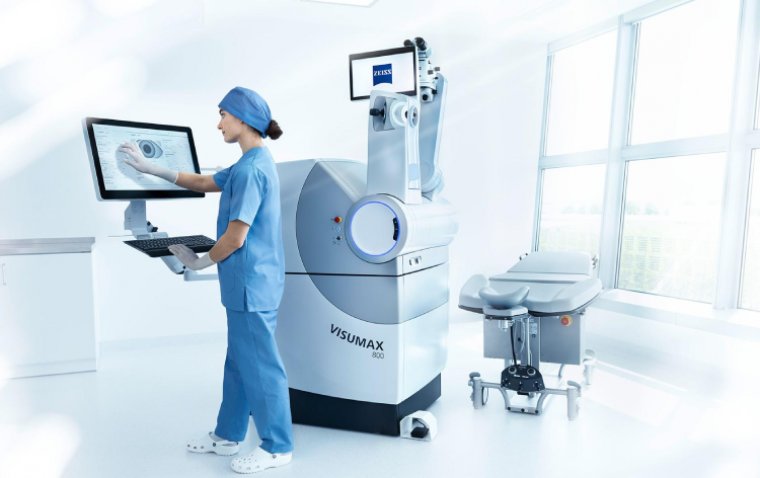
Управление по контролю качества пищевых продуктов и лекарственных средств США одобрило лазерную систему ZEISS VISUMAX® 800 с программным обеспечением SMILE® Pro для хирургической коррекции миопии
FDA одобрило фемтосекундную лазерную систему ZEISS VISUMAX® 800 с ПО SMILE® Pro для хирургии миопии и миопического астигматизма. Более 8 млн глаз в мире уже прооперированы по методике SMILE. Время …
Читать далее →
FDA одобрила проведение третьей фазы клинического исследования Ocuphire Pharma при снижении остроты зрения в условиях сумеречного освещения
Ocuphire Pharma получила одобрение FDA на проведение фазы 3 LYNX-2 для оценки эффективности офтальмологического раствора фентоламина при снижении остроты зрения в сумеречных условиях. Исследование охватило 200 пациентов в США, первичная …
Читать далее →